Les données de vie réelle à la base des diagnostics prédictifs développés par ACOBIOM

L’analyse des données de vie réelle (Real World Data ou RWD) permet d’obtenir des informations utiles et complémentaires aux données d’essais cliniques, et d’ajouter notamment certaines connaissances concernant l’utilisation de traitements ou de dispositifs médicaux dans la pratique clinique de routine.
Les données de vie réelle sont des données complémentaires des essais cliniques

Si les essais cliniques restent le gold-standard pour évaluer l’efficacité et la sécurité d’un traitement ou d’un diagnostic in-vitro, l’analyse des données de vie réelle constitue un complément précieux qui permet de vérifier la reproductibilité des résultats d’efficacité ou de tolérance d’un produit dans une population plus large et moins « sélectionnée » que celle des essais cliniques.
Les données de vie réelle (real world data) sont plurimodales, provenant de plusieurs sources (études cliniques observationnelles, dossiers médicaux numérisés, bases de données médico-administratives, enquêtes de santé, registres de patients, etc.), et souvent peu structurées.
Pourtant, les connaissances issues des analyses des RWD sont cruciales pour les acteurs de santé, notamment pour les autorités de santé, les centres hospitaliers et de soin, ainsi que les payeurs ou financeurs des systèmes de santé.
En effet, ces données renseignent sur la sécurité et le bon usage des traitements mis sur le marché car, en vie réelle, les patients ne sont pas « sélectionnés » comme dans les essais cliniques où sont appliqués des critères d’inclusion et d’exclusion.
L’intérêt est croissant pour les preuves issues « de la vraie vie » (Real World Evidence ou RWE), car les bases de données et méthodologies de recherche utilisées pour la collecte et l’analyse de ces données sont de plus en plus sophistiquées, et leurs utilisations de plus en plus demandées par les autorités de santé.
Aux Etats-Unis, la Food and Drug Administration (FDA) a ainsi créé le « FDA Real World Evidence Program Framework » afin d’évaluer l’utilisation de la RWE à tous les stades du processus de développement des médicaments, des diagnostics in-vitro et autres dispositifs médicaux. L’Agence européenne du médicament (European Medicines Agency ou EMA) a également montré son intérêt pour ce pan nouveau et inexploité des données médicales. Elle a reconnu que d’importantes questions médicales ou médico-économiques pourraient être étudiées via des analyses RWD (Learning Healthcare System).
Ces données de vie réelle sont collectées au sein des hôpitaux, des centres hospitaliers, des établissements de soins, ou même des cabinets de ville qui possèdent souvent des pratiques différentes dans leurs processus de collecte des données. Il est donc souvent nécessaire, pour garantir le succès d’un projet de type RWE, d’uniformiser ces données et/ou de les interpréter dans le contexte du système de santé dans lequel ces données ont été collectées.
Les études en vie réelle permettent ainsi d’identifier des sous-populations de patients, qui n’étaient pas incluses ou qui étaient sous-représentées dans les essais cliniques. Ces données peuvent aussi révéler des signaux de toxicité n’ayant pu être mesurés dans certains essais cliniques non calibrés et, dans cette hypothèse, auraient pu conduire à des restrictions d’AMM. Cependant, comme toute recherche, les analyses observationnelles et les analyses de données de vie réelle présentent certaines limites : elles peuvent identifier des corrélations entre certaines données, mais pas forcément de causalité.
Acobiom utilise les données de vie réelle
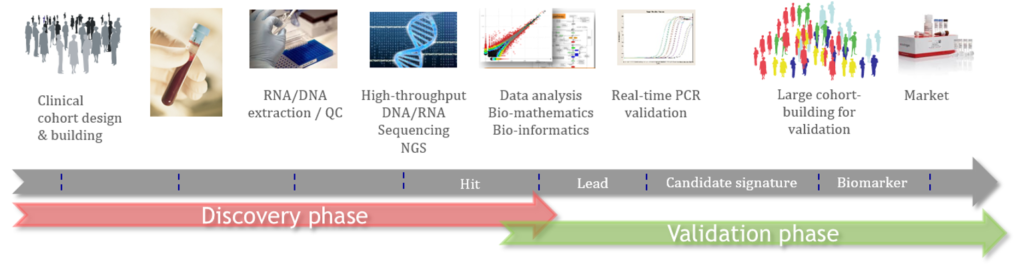
ACOBIOM utilise, compile et analyse ces approches RWD et RWE depuis de nombreuses années dans le développement de ses diagnostics, diagnostics compagnons et diagnostics prédictifs de réponse thérapeutique.
L’expertise de l’équipe scientifique de la société dans ces domaines s’est renforcée aux fils des années. Ainsi, les workflows d’analyses intégrées sont désormais matures et robustes, et permettent de produire des preuves scientifiques nécessaires à la mise sur le marché des diagnostics in-vitro de la société.
C’est le cas, par exemple, du GemciTest, diagnostic prédictif de la réponse thérapeutique à une thérapie à base de gemcitabine dans le traitement du cancer du pancréas. Ce diagnostic in-vitro a été mis au point suivant un processus d’élaboration basé sur l’analyse des données de vie réelle. Ce test identifie, parmi les patients diagnostiqués d’un adénocarcinome pancréatique métastatique, ceux qui ne présentent pas de bénéfice clinique en suivant un traitement de première intention à base de gemcitabine, seule ou en combinaison (cf : « Predictive Values of Blood-Based RNA Signatures for the Gemcitabine Response in Advanced Pancreatic Cancer », Piquemal et al. Cancers 2020).
La population de patients identifiée par le GemciTest peut ainsi être précocement orientée vers une alternative thérapeutique à la gemcitabine.
Grâce à ces approches RWD et RWE, et à l’utilisation de sources robustes de données cliniques et biologiques, ACOBIOM peut ainsi contribuer à de meilleures prises de décisions thérapeutiques sur la base du suivi de patients dans la pratique courante.

